Fecha de recepción: 29-05-2025
Fecha de aceptación: 28-06-2025
DOI: 10.24875/KRANION.M25000108
Disponible en internet: 22-08-2025
Kranion. 2025;20(Supl 1):4-11
Introducción
La migraña representa la segunda causa global de años vividos con discapacidad, afecta a más del 10% de la población mundial en edad productiva1. Esta cefalea primaria, cuya fisiopatología implica una compleja interacción entre mecanismos neurovasculares y neuroinflamatorios, se manifiesta con episodios recurrentes que deterioran significativamente la calidad de vida del paciente.
El tratamiento sintomático es fundamental en la atención del paciente con migraña, ya que permite abortar o atenuar los ataques y reducir su impacto funcional. La situación actual de su tratamiento en nuestro país sigue siendo precaria, con un 30% de pacientes no tratados2 y solo un 39-44,1% usando triptanes2,3. A lo largo de las últimas décadas se han desarrollado múltiples opciones terapéuticas, entre las que destacan los antiinflamatorios no esteroideos (AINE), los más usados2,3; los triptanes, hasta hace no mucho el tratamiento más específico; las combinaciones farmacológicas dirigidas a múltiples dianas, y los nuevos fármacos más selectivos y mejor tolerados. Sin embargo, persisten desafíos clínicos como la respuesta insuficiente, los efectos adversos, la falta de formación en atención primaria o las contraindicaciones, especialmente en pacientes con comorbilidades.
En este contexto, la International Headache Society (IHS) ha publicado recientemente una guía global de recomendaciones clínicas basada en la evidencia para el tratamiento farmacológico agudo de la migraña1,4 que actualiza y sistematiza el uso de los fármacos disponibles. Esta revisión narrativa tiene como objetivo analizar dichas recomendaciones, explorar las opciones terapéuticas actuales (con énfasis en la combinación de sumatriptán/naproxeno, ampliamente respaldada por la evidencia)5,6 y destacar aspectos clave para la selección individualizada del tratamiento sintomático.
Bases del tratamiento agudo de la migraña
El tratamiento agudo de la migraña tiene como objetivo principal interrumpir el ataque en curso, aliviar el dolor y los síntomas acompañantes, y restablecer la funcionalidad del paciente con la mayor rapidez y seguridad posibles, en las primeras dos horas y manteniendo el efecto 24 h7. Esto coincide con las preferencias de los pacientes8. Para lograrlo es fundamental intervenir de forma temprana, idealmente durante la primera hora del ataque9–1, cuando la sensibilización central aún no se ha establecido completamente (alodinia), e informar de manera adecuada para generar confianza y evitar falsas expectativas8. Algo muy relevante y que la mayoría ignora es que el tratamiento debe ser estratificado, no escalonado. Es decir, si tenemos una crisis grave, debemos tratarla directamente con un triptán y no esperar que un AINE la resuelva.
Desde el punto de vista fisiopatológico, la migraña se origina en una disfunción del sistema trigeminovascular, con activación de fibras aferentes que liberan neuropéptidos proinflamatorios como el péptido relacionado con el gen de la calcitonina (CGRP), sustancia P y neuroquinina A. Estos eventos provocan vasodilatación, neurogénesis del dolor y un proceso inflamatorio estéril en las meninges. A esto se suma una modulación alterada a nivel del tronco encefálico y del tálamo que contribuye a la percepción del dolor y a los síntomas neurológicos asociados.
Los fármacos empleados en el tratamiento agudo buscan interferir con estos mecanismos, ya sea mediante la inhibición de la transmisión nociceptiva, la modulación de la vasodilatación o el bloqueo de neurotransmisores clave. La elección del agente terapéutico debe tener en cuenta la intensidad de la crisis (tratamiento estratificado), la presencia de náuseas o vómitos, la rapidez deseada del efecto, las experiencias previas del paciente y la existencia de comorbilidades médicas. Dado el arsenal terapéutico actualmente disponible, se propone en primera instancia dividir a los pacientes en dos grupos: con o sin afección cardiovascular activa (Fig. 1).
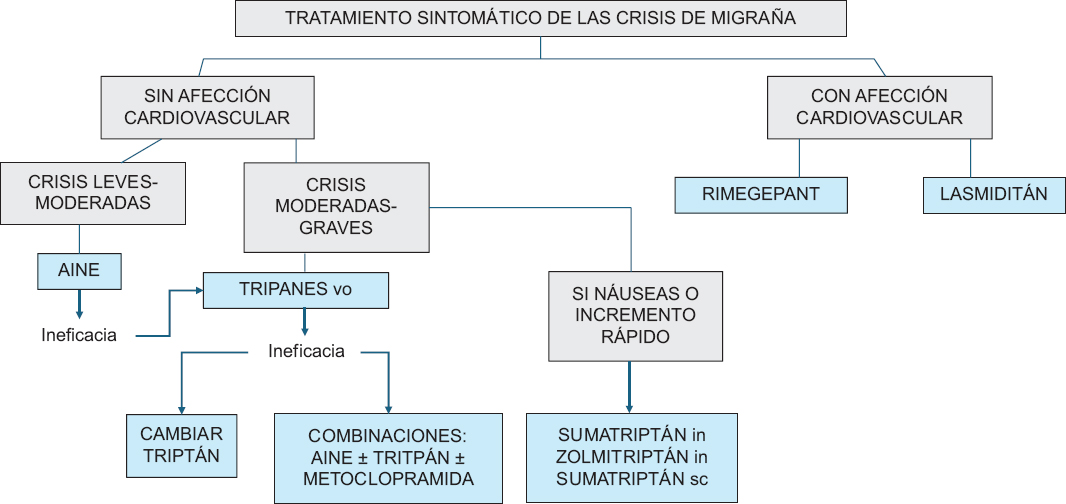
Figura 1. Tratamiento sintomático de las crisis de migrañas. Propuesta según la evidencia actual. vo: vía oral; in: vía intranasal; sc: vía subcutánea.
La IHS propone un enfoque estratificado en el que la intensidad y características del ataque determinan la selección inicial del tratamiento1. Los pacientes con crisis leves a moderadas pueden beneficiarse del uso de AINE o analgésicos simples, mientras que aquellos con ataques más graves o con respuesta subóptima previa pueden requerir triptanes u otras opciones más específicas.
Un aspecto clave en la eficacia del tratamiento agudo es la administración temprana, preferiblemente dentro de la primera hora desde el inicio de los síntomas. También se recomienda evitar el uso excesivo de medicación, ya que el abuso de fármacos sintomáticos está asociado a un mayor riesgo de cronificación de la migraña.
Fármacos disponibles para el tratamiento agudo de la migraña
El tratamiento agudo de la migraña se basa en una variedad de opciones farmacológicas cuya elección depende de la intensidad de la crisis, la presencia de síntomas asociados y las características individuales del paciente. Recientemente, la IHS ha revisado los grados de evidencia de cada uno de ellos4 (Tabla 1).
Table 1. Resumen de las recomendaciones para el tratamiento de las crisis de migraña según calidad de la evidencia, grado de la recomendación y eficacia comparativa24
| Tratamiento | Calidad de la evidencia | Fuerza de la recomendación | Comentario sobre eficacia comparativa |
|---|---|---|---|
| Rizatriptán 10 mg | Alta/baja | Fuerte/débil | Superior a ibuprofeno y ergotamina en estudios comparativos |
| Eletriptán 20-40 mg | Alta | Fuerte | Superior a sumatriptán |
| Frovatriptán 2,5 mg + dexketoprofeno 37,5 mg | Moderada | Débil | Superior a frovatriptán solo |
| Sumatriptán (oral, intranasal, subcutáneo; 50-100 mg) | Alta/muy baja | Fuerte/débil | Eficacia variable según dosis y comparador |
| Paracetamol 1.000 mg | Alta/baja | Fuerte/débil | Menor eficacia comparado con triptanes |
| Paracetamol 500 mg + AAS 500 mg + cafeína 130 mg | Alta | Fuerte | Combinación más eficaz que monoterapia |
| AAS 900-1.000 mg ± metoclopramida 10 mg | Moderada | Fuerte | Alta eficacia, especialmente en combinación |
| Zolmitriptán 2,5 mg | Alta | Fuerte | No comparado directamente en estudios head to head |
| Lasmiditán 50-200 mg | Alta | Fuerte | Alternativa efectiva no triptán; sin comparaciones directas |
| Rimegepant 75 mg Ubrogepant 50-100 mg | Alta | Fuerte | Antagonistas CGRP, evidencia creciente |
| Zavegepant 10 mg intranasal | Alta | Fuerte | Alternativa intranasal, sin comparaciones directas |
| Diclofenaco 50 mg (oral o subcutáneo) | Moderada/baja | Fuerte/débil | Útil en contexto de AINE |
| Ibuprofeno 200-600 mg | Baja | Fuerte/débil | Menor eficacia comparado con triptanes |
| Naproxeno 500-825 mg | Muy baja | Fuerte/débil | Limitada eficacia como monoterapia |
| Ergotamina 2 mg + cafeína 200 mg | Moderada/muy baja | Fuerte | Inferior a triptanes en la mayoría de los estudios comparativos |
| Prometazina 25 mg + sumatriptán 50 mg | No especificado | No especificado | Mejor que sumatriptán solo en comparaciones limitadas |
| Trimebutina 200 mg + rizatriptán 10 mg | No especificado | No especificado | Combinación potencialmente superior a monoterapia |
| Paracetamol 1.000 mg + rizatriptán 10 mg | Baja | Débil | Combinación menos eficaz que otras opciones |
| Carbasalato de calcio 900 mg + metoclopramida 10 mg | No especificado | No especificado | Alternativa poco documentada |
|
AAS: ácido acetilsalicílico; AINE: antiinflamatorio no esteroideo; CGRP: péptido relacionado con el gen de la calcitonina. Adaptada de Láinez et al., 200742. |
|||
Analgésicos simples y antiinflamatorios no esteroideos
Los analgésicos simples, como el paracetamol, y los AINE, como el ibuprofeno, el naproxeno y el naproxeno sódico, son comúnmente utilizados en crisis de migraña de leve a moderada intensidad. Su eficacia se atribuye a la inhibición de la síntesis de prostaglandinas, reduciendo así la inflamación y el dolor. Sin embargo, su empleo frecuente puede conllevar el desarrollo de una cefalea por uso excesivo de medicación, por lo que se recomienda limitar su uso a menos de 15 días al mes para evitar este riesgo.
El paracetamol (acetaminofeno) tiene un bajo perfil de eficacia a pesar de usarse con frecuencia. Si se combina con otros tratamientos se debe restringir a menos de 10 días al mes. Es seguro durante el embarazo.
El metamizol se emplea en abundancia en nuestro medio a pesar de existir poca evidencia de eficacia y tener descritos importantes eventos adversos, siendo el más común la hipotensión arterial. Su uso está lleno de controversias a las que la población es ajena12.
Los AINE deben emplearse a dosis altas e incluso de carga de forma precoz, por ejemplo: ibuprofeno: 600-1.200 mg, naproxeno sódico: 550-1.100 mg. El segundo tiene mejor perfil cardiovascular. Su eficacia se relaciona con el tiempo que tardan en alcanzar su concentración máxima (Tmáx): ibuprofeno < 2 h, naproxeno < 2 h y dexketoprofeno < 0,5 h. La vida media de naproxeno es de hasta 15-17 h, siendo en el resto de apenas 2 h13. Los COX2, como meloxicam o celecoxib, producen menos complicaciones hemorrágicas.
Antieméticos y otros adyuvantes
La metoclopramida y la domperidona se usan de manera regular en las crisis de migraña, generalmente como antieméticos, aunque al mejorar la absorción de los fármacos asociados potencian su efecto. Al inhibir las vías dopaminérgicas no solo eliminan las náuseas, sino también el dolor y los síntomas asociados, razón por la que el primero se puede emplear en su formulación intravenosa en monoterapia para controlar el ataque. La metoclopramida atraviesa la barrera hematoencefálica, por lo que puede producir efectos extrapiramidales y asocia con más frecuencia hipotensión arterial. La domperidona puede prolongar el intervalo QT con más frecuencia14.
Triptanes
Los triptanes, como el sumatriptán, el rizatriptán y el eletriptán, el zomitriptán o el almotriptán, son agonistas selectivos de los receptores 5-HT1B/1D y representan, hoy en día, la opción más eficaz para el tratamiento de las crisis de migraña moderadas a graves, aunque la metodología para demostrarlo ha sido controvertida15. Su mecanismo de acción incluye la vasoconstricción de los vasos craneales dilatados y la inhibición de la liberación de neuropéptidos proinflamatorios, entre ellos el CGRP. Es importante destacar que la administración temprana, preferiblemente al inicio del dolor, mejora significativamente su eficacia. En la recaída precoz puede administrarse una segunda dosis del mismo triptán, y si vuelve a recaer, deberá cambiarse a un triptán de vida media más larga1. Cada triptán es distinto, ya que tienen diferencias farmacocinéticas y farmacodinámicas16–18.
Su mayor problema es la tolerabilidad19, según se ha observado en los estudios de satisfacción terapéutica3. Pese a ser el tratamiento de elección por su eficacia, persiste un miedo infundado a su uso20. En general, el uso de triptanes no parece incrementar el riesgo vascular21, pero en la población con más riesgo cardiovascular puede aumentarlo22. Por ello están contraindicados en caso de enfermedad coronaria, cerebrovascular y vascular periférica, hipertensión mal controlada y toma de ergóticos durante las 24 h previas23,24. En la migraña hemipléjica y del troncoencéfalo la contraindicación parece infundada25,26. El aura no contraindica su uso y existe controversia en cuanto a su utilidad durante esta para evitar las crisis de dolor27,28. El incremento de síndrome serotoninérgico en caso de asociación de estos fármacos con inhibidores de la recaptación de serotonina es anecdótico29, y la alarma generada por la Food and Drug Administration (FDA)30 parece infundada.
En caso de respuesta parcial, se recomienda verificar si la toma es correcta, aumentar la dosis o cambiar de triptán1. Si la situación persiste, se puede asociar AINE o antieméticos e incluso valorar tratamiento preventivo. Para determinar si un triptán es eficaz debe haber respuesta satisfactoria a tres de cuatro usos. Se consideran resistentes aquellos pacientes que no responden a dos clases de triptanes y refractarios a tres7. En caso de fallo a tres clases de triptanes se optará por analgésicos1. Existen factores que predicen la no respuesta31 y la respuesta32 a estos medicamentos. En general, los no respondedores son pacientes crónicos con migraña de larga duración e importantes comorbilidades asociadas, como obesidad y depresión.
Combinaciones farmacológicas: sumatriptán/naproxeno
La combinación de sumatriptán y naproxeno ha demostrado ser más eficaz que la administración de cada uno por separado en el tratamiento agudo de la migraña. Esta combinación aprovecha los mecanismos complementarios de ambos fármacos: el sumatriptán actúa en los receptores serotoninérgicos, mientras que el naproxeno inhibe la síntesis de prostaglandinas. Diversos estudios han mostrado que esta combinación mejora la eficacia terapéutica y reduce la recurrencia del dolor4–5.
Ditanes
El lasmiditán es un agonista selectivo de los receptores serotoninérgicos 5HT1F. Es eficaz para el control del dolor desde los primeros 30 min hasta las 4 h, independiente del fracaso previo a triptanes. Es un fármaco seguro en pacientes cardiovasculares. En nuestro medio está financiado en caso de migraña con y sin aura con más de tres crisis al mes y fallo o contraindicación a al menos dos triptanes. Existen tres presentaciones (50, 100 y 200 mg). La dosis de inicio es de 100 mg/día. Al atravesar la barrera hematoencefálica produce mareo hasta en un 30% de los casos, por lo que se debe evitar conducir hasta 8 h tras la toma33–38.
Gepantes
Los gepantes son antagonistas del receptor del CGRP. En España solo está disponible el rimegepant, indicado como tratamiento agudo en caso de fallo o mala tolerancia a más de dos triptanes. Se presenta en dosis de 75 mg en cajas de 2-8 comprimidos. La evidencia actual respalda que es seguro en pacientes con enfermedad cardiovascular y no produce cefalea de rebote por el uso excesivo, a diferencia de los triptanes. En general se tolera bien, pero su mayor ventaja es que al ser eficaz también como preventivo (toma a días alternos), baja la frecuencia de la migraña39 y reduce el consumo de otros tratamientos sintomáticos40.
Neuromodulación
Existen varios dispositivos que tienen indicación como tratamiento sintomático de la migraña: estimulación no invasiva del nervio vago, estimulación transcraneal del nervio supraorbitario, estimulación magnética transcraneal de pulso simple y estimulación eléctrica remota. Sin embargo, la evidencia que abogue por su efectividad es baja, y tan solo la última opción dispone de estudios de mayor solidez.
Evidencia clínica y eficacia comparada de los tratamientos agudos
La evidencia clínica acumulada en las últimas décadas ha permitido establecer un perfil de eficacia y seguridad bien definido para los fármacos empleados en el tratamiento sintomático de la migraña. Las guías más recientes, como las recomendaciones globales de la IHS, integran múltiples revisiones sistemáticas y metaanálisis para jerarquizar la utilidad clínica de cada opción terapéutica1–4,.
AINE y triptanes: eficacia y limitaciones
Los AINE, como naproxeno e ibuprofeno, se sitúan entre los fármacos de primera línea para crisis de leve a moderada intensidad. Su eficacia ha sido demostrada en múltiples estudios controlados, con tasas de alivio del dolor a las 2 h entre el 40 y el 60%41. No obstante, su efecto suele ser más modesto en ataques de mayor intensidad o en pacientes con síntomas vegetativos marcados.
Por otro lado, los triptanes han demostrado tasas de alivio del dolor a las 2 h superiores al 60%, con una eficacia sostenida en el tiempo y una reducción de la recurrencia en muchos casos. Tal como se ha comentado más arriba, se considera que un triptán es eficaz si hay respuesta en tres de cuatro intentos7. En particular, el sumatriptán oral a dosis de 100 mg ha sido uno de los más ampliamente estudiados, con efectos significativos sobre el dolor, las náuseas y la fotofobia1–41. Sin embargo, al igual que otros triptanes, su empleo puede verse limitado por efectos adversos (como parestesias, opresión torácica) y contraindicaciones cardiovasculares.
Combinación sumatriptán/naproxeno: sinergia terapéutica
Diversos ensayos clínicos y metaanálisis han respaldado la superioridad de la combinación de sumatriptán 85 mg con naproxeno sódico 500 mg frente al uso individual de cada componente. Esta combinación proporciona un alivio del dolor significativamente mayor a las 2 y 24 h, además de reducir la necesidad de medicación de rescate y la tasa de recurrencia del ataque4–5.
En el metaanálisis de Syed (2016) se documentó que la combinación era consistentemente más efectiva que el placebo y que los componentes por separado, tanto para el alivio del dolor como para la normalización funcional5. En una revisión más reciente de Wilcha et al. (2024) se reafirman estos hallazgos, destacando su utilidad en ataques moderados a graves y su buena tolerancia en la mayoría de los pacientes4.
Este efecto sinérgico puede explicarse por la acción combinada sobre diferentes vías fisiopatológicas de la migraña: mientras el sumatriptán actúa a nivel serotoninérgico con efecto vasoconstrictor y antinociceptivo, el naproxeno contrarresta la inflamación meníngea y la sensibilización central.
Nuevas moléculas: gepantes y ditanes
El desarrollo de nuevos agentes como los gepantes (ubrogepant, rimegepant) y los ditanes (lasmiditán) ha ampliado el arsenal terapéutico disponible, especialmente en aquellos pacientes que no pueden usar triptanes. Los gepantes han demostrado eficacia comparable en términos de alivio del dolor, con una menor incidencia de efectos adversos y sin las contraindicaciones cardiovasculares que limitan el uso de triptanes42. Sin embargo, su acceso aún es limitado en muchos países y su coste es generalmente mayor. Las guías actuales sugieren considerar su uso en pacientes con contraindicación o mala tolerancia a los triptanes, o en quienes no han respondido adecuadamente a estos fármacos1.
Consideraciones para la individualización del tratamiento
El abordaje terapéutico de la migraña no debe ser uniforme. Dada la gran heterogeneidad clínica de los pacientes y de las crisis o ataques, se impone la necesidad de una estrategia individualizada que contemple no solo la intensidad del dolor, sino también el perfil sintomático, la frecuencia de las crisis, la comorbilidad asociada y las preferencias del paciente.
Tipo de crisis y características clínicas
Los pacientes con crisis infrecuentes, bien delimitadas y de intensidad leve pueden responder adecuadamente a analgésicos simples o AINE. Por el contrario, quienes experimentan crisis de inicio rápido, con síntomas vegetativos intensos (náuseas, vómitos, fotofobia) o con aura, suelen requerir triptanes o terapias combinadas desde el inicio. En estos casos, la rapidez de acción y la eficacia sostenida son factores clave para restaurar la funcionalidad.
Comorbilidades médicas
Los pacientes con migraña tienen de 1,2 a 2,2 más prevalencia de comorbilidades2. Las enfermedades cardiovasculares (cardiopatía isquémica, hipertensión no controlada, antecedentes de ictus) constituyen una contraindicación para el uso de triptanes, por lo que alternativas como los gepantes, los ditanes o las combinaciones de AINE más antieméticos cobran especial relevancia. Asimismo, los pacientes con trastornos gastrointestinales que dificultan la absorción oral pueden beneficiarse de formulaciones intranasales, subcutáneas o rectales.
En el caso de pacientes con ansiedad o trastornos depresivos conviene evitar tratamientos que puedan potenciar efectos centrales adversos. Además, la coexistencia de cefalea por uso excesivo de medicación obliga a un manejo más cuidadoso del tratamiento sintomático y a considerar con mayor firmeza opciones preventivas.
Respuesta previa y adherencia
La experiencia previa del paciente con ciertos fármacos es un excelente predictor de respuesta futura. Por ello se recomienda siempre documentar la eficacia, duración del alivio, presencia de recurrencias y tolerabilidad de cada tratamiento empleado. Esto facilita decisiones futuras, especialmente al introducir nuevas combinaciones o al optar por escalamiento terapéutico.
El uso de combinaciones como sumatriptán/naproxeno ha mostrado no solo una mayor eficacia, sino también un mejor perfil de satisfacción y adherencia por parte del paciente, lo que puede influir en la reducción del consumo excesivo y mejorar el control global de la enfermedad4,5.
Accesibilidad y educación del paciente
La disponibilidad de ciertos medicamentos puede estar condicionada por factores regulatorios o económicos. En muchos países, los gepantes aún no están disponibles o son de elevado coste. En este contexto, educar al paciente sobre el uso racional de los tratamientos disponibles y la importancia de administrarlos de forma precoz es esencial para optimizar los resultados clínicos.
Los programas de educación terapéutica deben enfatizar la identificación temprana de los pródromos, la selección del tratamiento más adecuado para cada tipo de crisis, y los signos de alerta para reevaluar la estrategia si esta resulta inefectiva.
Conclusiones
El tratamiento farmacológico de las crisis de migraña ha evolucionado significativamente en las últimas décadas, permitiendo un abordaje más eficaz y personalizado. La elección del fármaco debe basarse en la intensidad y características del ataque, así como en las comorbilidades y preferencias del paciente. Aunque los AINE y los triptanes siguen siendo los pilares terapéuticos, combinaciones como sumatriptán/naproxeno han demostrado superioridad en eficacia y perfil de tolerabilidad. La irrupción de nuevos fármacos, como los gepantes y ditanes, ofrece alternativas prometedoras, especialmente en pacientes con limitaciones para el uso de triptanes. Un tratamiento precoz, racional y adaptado al perfil del paciente es fundamental para optimizar el control de la enfermedad, mejorar la calidad de vida y prevenir la cronificación. La actualización constante del conocimiento clínico y la educación terapéutica del paciente son herramientas clave en este proceso.
Financiación
El presente trabajo no ha recibido ninguna subvención oficial, beca o apoyo de un programa de investigación destinados a la redacción de su contenido.
Conflicto de intereses
El autor no comunica conflicto de intereses en relación con el contenido del trabajo.
Consideraciones éticas
Protección de personas y animales. El autor declara que para este trabajo no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad, consentimiento informado y aprobación ética. El estudio no involucra datos personales de pacientes ni requiere aprobación ética. No se aplican las guías SAGER.
Declaración sobre el uso de inteligencia artificial. El autor declara que no utilizó ningún tipo de inteligencia artificial generativa para la redacción de este manuscrito.