INTRODUCCIÓN
El uso de la inteligencia artificial (IA) es ya una realidad en muchas enfermedades, y el estudio y tratamiento de las cefaleas no son una excepción. La alta prevalencia de las cefaleas y el estigma que las acompaña en muchas ocasiones representan una oportunidad para que las herramientas digitales atiendan a grandes poblaciones de pacientes que además pueden no sentirse cómodos buscando la atención médica adecuada y necesaria para su dolor1. Entre los principales usos más estudiados hasta el momento se encuentran: el diagnóstico diferencial de las distintas entidades, la detección precoz o predicción de las crisis de dolor y la predicción de la respuesta terapéutica (Tabla 1).
TABLA 1. Principales aplicaciones de la inteligencia artificial en el campo de las cefaleas
| Aplicaciones | Principales resultados hasta la fecha |
|---|---|
| Diagnóstico | – Existe una alta concordancia en el diagnóstico de migraña mediante entrevistas clínicas virtuales frente a la entrevista clínica real2 |
| – Las aplicaciones móviles con registro en tiempo real de características clínicas han definido 4 tipos diferentes de crisis de dolor en migraña3 | |
| – Algunos aspectos del lenguaje pueden diferenciar la fase interictal de la premonitoria de la crisis de migraña4 | |
| – El procesamiento del lenguaje natural y los algoritmos de aprendizaje automático permiten diferenciar pacientes con cefalea en racimos y migraña según los términos utilizados para describir su dolor5 | |
| – Las técnicas de IA pueden detectar asociaciones en factores desencadenantes y características sociodemográficas de la cefalea por uso excesivo de medicación6 | |
| Pruebas complementarias | – La resonancia magnética estructural y funcional combinada con IA puede clasificar a pacientes con migraña con alta precisión7–10 |
| – El estudio del conectoma utilizando IA permite identificar marcadores de migraña y diferenciarla de otras enfermedades que cursan con dolor crónico11 | |
| – El electroencefalograma y la magnetoencefalografía pueden servir como biomarcadores para diferenciar migraña con y sin aura12,13 | |
| Predicción de crisis de migraña | – Los modelos de IA pueden predecir con alta precisión la fase de dolor en migraña si se combinan con dispositivos portátiles para el registro de variables biométricas en tiempo real14–16 |
| – Las aplicaciones móviles han permitido recopilar grandes cantidades de datos clínicos y no clínicos (p. ej., tiempo atmosférico) que facilitan la predicción de crisis de migraña17 | |
| – El electroencefalograma en estado de reposo puede ayudar en la detección de fases preictales de la migraña18 | |
| Predicción de respuesta a fármacos | – La IA aplicada a datos clínicos y de neuroimagen puede predecir respuesta terapéutica en migraña y cefalea en racimos19–21 |
|
IA: inteligencia artificial. |
|
INTELIGENCIA ARTIFICIAL PARA EL DIAGNÓSTICO DE LA CEFALEA
El diagnóstico de la cefalea es fundamentalmente clínico, basado en la anamnesis. Se puede considerar complejo en la medida en que se basa fundamentalmente en síntomas y signos clínicos que han de ser frecuentemente descubiertos mediante anamnesis dirigida. Dada la complejidad y heterogeneidad de las distintas cefaleas, los síntomas que ocurren antes, durante y después de las crisis de dolor pueden ser descritos de distintas formas por cada paciente5. Además, el gold standard actual para su diagnóstico, los criterios de la tercera edición de la clasificación internacional de cefaleas (CIC-3), son útiles para el diagnóstico de los cuadros típicos, pero para dolores atípicos es a menudo el enfoque subjetivo del médico especialista y su experiencia lo que define el mejor diagnóstico22. Pese a ello, las distintas técnicas de IA están ganando terreno en la época de telemedicina actual, ya que pueden ahorrar el tiempo que normalmente se dedica a una entrevista médica, a la vez que mejoran la precisión diagnóstica23.
Aplicabilidad de la IA en el diagnóstico clínico de la cefalea
Un buen sistema de diagnóstico automatizado en cefaleas debería ser capaz, al menos, de diferenciar las distintas cefaleas primarias, reconocer el uso excesivo de medicación y detectar características de riesgo de una peor evolución de la enfermedad24.
Una revisión sistemática reciente que incluye los 41 estudios realizados hasta junio de 2021 que habían evaluado herramientas computarizadas/automáticas para el diagnóstico de migraña encontró que el 60% de estas herramientas se desarrollaron con base en los criterios de la CIC-3, la mitad fueron autoadministrados y más del 80% utilizaron entrevistas clínicas presenciales como método comparativo. La mediana de precisión diagnóstica fue del 89%, con una sensibilidad del 87% y una especificidad del 90%, si bien en el 95% de los estudios no existió un muestreo aleatorizado de los pacientes1.
Migraña
La concordancia entre el diagnóstico online, autoadministrado y basado en un motor de diagnóstico computacional y una entrevista semiestructurada clínica podría ser excelente a la hora de diagnosticar migraña y probable migraña, con unas tasas de especificidad y de valor predictivo positivo cercanas al 90%2.
Las técnicas de IA también permiten analizar el lenguaje espontáneo del paciente con migraña. Es posible clasificar pacientes con migraña frente a pacientes con cefalea en racimos de acuerdo con los términos utilizados durante la descripción espontánea de su dolor con técnicas de procesamiento del lenguaje natural y algoritmos de aprendizaje automático5. También se ha evidenciado la existencia de una alteración en la velocidad del habla, la duración de la fonación y/o la precisión de la articulación entre la fase interictal y la fase premonitoria de la crisis de migraña en casi la mitad de los pacientes con migraña sin aura4.
Otra posible utilidad de las técnicas de IA en el manejo diagnóstico de la migraña sería identificar a aquellos pacientes con una cefalea de mayor gravedad, al poder incluir en los algoritmos de aprendizaje automático variables tradicionalmente no relacionadas con el dolor25.
Recientemente, el uso de una aplicación móvil con registro en tiempo real de las características clínicas del dolor ha permitido clasificar la fase de dolor de la crisis de migraña en cuatro tipos3.
Otras cefaleas primarias
En 2007, el sistema CHAT surgió como un programa de ordenador útil y experto en el diagnóstico de las cefaleas primarias y de la cefalea por uso excesivo de medicación analgésica. Como principal limitación, esta técnica mostró que era necesario que el paciente fuera preciso en sus respuestas, siendo más probable que una entrevista personal obtenga este tipo de respuestas. Además, el programa no permitía generar un diagnóstico con más de un tipo de dolor. Por ello se propuso que su principal utilidad era como método de cribado antes de la entrevista médica24.
La evolución de la tecnología de los últimos años y su combinación con aplicaciones móviles, aplicaciones web y técnicas de aprendizaje automático ha permitido mejorar la fiabilidad de este tipo de sistemas. En la era en la que la mayor parte de los pacientes tienen acceso inmediato a un teléfono inteligente con red de internet se puede facilitar el registro de las crisis de dolor y de la medicación utilizada en cualquier momento y lugar22.
La viabilidad de las técnicas de IA en el desarrollo de estrategias de clasificación automatizada en las cefaleas primarias está siendo continuamente analizada, sin ser capaces de reemplazar el diagnóstico médico en muchos de los casos. Sin embargo, es posible que estas técnicas detecten características diferenciales de los tipos de dolor, no recogidos en la actual clasificación, como son el modo de inicio, las características demográficas y la cualidad del dolor26.
Los algoritmos artificiales de clasificación inmunes pueden aumentar la precisión diagnóstica de los sistemas clásicos de IA hasta un 95-99% a expensas de una pérdida de especificidad por la baja representación de las cefaleas más inhabituales27.
Los sistemas de diagnóstico basados en IA pueden ser especialmente útiles en la consulta de los médicos de atención primaria, que deben clasificar diferentes enfermedades, estableciendo grados de certeza y de posible gravedad según una serie de signos y síntomas. Este tipo de abordaje es similar al usado por muchos de los métodos de aprendizaje automático, cuya precisión diagnóstica podría ser algo superior a la de los médicos no especialistas28. Estos modelos de diagnóstico se han ensayado con datos de hasta 4.000 pacientes y resultados satisfactorios23.
Cefalea por uso excesivo de medicación analgésica
La cefalea por uso excesivo de medicación analgésica (CUEM) resulta una entidad especialmente atractiva en el contexto de la medicina predictiva, ya que muchos de sus factores desencadenantes (exposición a fármacos, estilo de vida, características sociodemográficas) son rutinariamente recogidos en las historias clínicas electrónicas. Las técnicas de aprendizaje automático, en especial si se combinan con vectores de soporte y optimización aleatoria, permiten una ponderación de la importancia relativa de los diferentes atributos y detectar asociaciones más generales y poco analizadas hasta el momento6.
Aplicabilidad de la IA en el diagnóstico mediante pruebas complementarias en migraña
Resonancia magnética estructural y funcional
El primer estudio que mostró la posible utilidad de la resonancia magnética estructural en la clasificación de controles sanos y pacientes con migraña episódica y crónica data de 2015. En él se utilizaron métodos de clasificación cruzada secuencial con clasificadores que contenían varias medidas estructurales del polo temporal, la corteza cingulada anterior, el lóbulo temporal superior, la corteza entorrinal, la circunvolución frontal orbital medial y la pars triangularis7.
Estudios posteriores han tratado de mejorar la posibilidad de clasificar pacientes con migraña al aunar técnicas como el tensor de difusión (DTI) y pruebas psicológicas junto con técnicas de aprendizaje automático. Se obtendría un 93% de precisión con tres clasificadores que contendrían las siete características más importantes de las imágenes DTI y datos relacionados con la emoción y cognición8.
La conectividad funcional en reposo de las regiones temporal media derecha, insular posterior, cingulada media, prefrontal ventromedial izquierda y amigdalar bilateral podría ser otro marcador diferenciador del cerebro con migraña del cerebro sano con una precisión algo superior al 86%. Esta diferencia sería mayor en pacientes con un mayor tiempo de evolución de la enfermedad9. Otras técnicas de IA, como Inception, aumentarían la precisión de la resonancia magnética funcional en estado de reposo hasta casi el 99% para el diagnóstico de pacientes con migraña10.
Es precisamente el estudio del conectoma, entendido como el estudio de las redes o los sistemas cerebrales y no de las estructuras cerebrales individuales, el que se ha ido posicionando como la parte más importante en la fisiopatología de la migraña. Un estudio multinivel que utilizó un enfoque de aprendizaje automático y de conectividad funcional en estado de reposo de todo el cerebro permitió identificar un marcador neuronal con conectividad funcional anormal dentro de varias redes que permitía discriminar a los pacientes con migraña con una sensibilidad del 93% y una especificidad del 89%, incluso frente a otros trastornos que cursan con dolor crónico (fibromialgia y dolor lumbar crónico)11.
Aún más recientemente, la combinación de la espectroscopia funcional cercana al infrarrojo con el aprendizaje automático habría demostrado poder diferenciar con una alta sensibilidad y especificidad a los pacientes con migraña crónica de aquellos con CUEM y de controles sanos gracias a los cambios en la hemoglobina de la corteza prefrontal durante una tarea de aritmética29.
Electroencefalografía
Un estudio realizado durante el estado de reposo con electroencefalografía ha mostrado que una métrica de conectividad funcional de los datos electroencefalográficos podría servir como biomarcador para diferenciar entre migraña con y sin aura con una precisión del 84,62%12.
Magnetoencefalografía
En comparación con la electroencefalografía convencional, la magnetoencefalografía es superior a la hora de localizar y medir la actividad cortical. Esto ha permitido estudiar la participación de redes corticales superiores multisensoriales en el procesamiento del dolor. Un estudio con datos magnetoencefalográficos en estado de reposo que incluyó a 135 pacientes con migraña (100 migraña crónica y 35 migraña episódica), 70 controles sanos y 35 pacientes con fibromialgia, observó diferencias en las interacciones funcionales en las redes sensitivomotoras y por defecto en los pacientes con migraña crónica frente a controles sanos y migraña episódica con una precisión del 86,8 y el 94,5%, respectivamente13.
INTELIGENCIA ARTIFICIAL EN LA PREDICCIÓN DE CRISIS DE MIGRAÑA
En muchos pacientes, la aparente impredictibilidad de las crisis de dolor conlleva síntomas de ansiedad, con mayor deterioro funcional. La estrategia actual de los tratamientos sintomáticos es su toma precoz una vez iniciado el dolor. El 67,6% de los pacientes son capaces de predecir al menos una crisis de dolor, pero solo algo más de un tercio de ellos pueden ser considerados buenos predictores (detección de más del 50% de las crisis)30.
Poder predecir la fase de dolor ha cobrado especial importancia en los últimos años. Así, los factores desencadenantes, los síntomas premonitorios y los cambios fisiológicos que ocurren en la fase premonitoria pueden usarse en modelos predictivos de ataques. El aprendizaje automático es una opción prometedora para tales análisis predictivos, más en su uso combinado con dispositivos portátiles capaces de detectar variables biométricas en tiempo real14.
La aplicación de modelos de predicción personalizados que utilizaban memoria a corto plazo de redes neuronales artificiales recurrentes a los datos obtenidos de estos registros ha sido capaz de generar un algoritmo de predicción de la fase de dolor preciso en el 95% de las crisis15,16 (Fig. 1). El inconveniente de este tipo de modelos es la necesidad de usar el dispositivo a lo largo de todo el día, ya que el registro exclusivamente nocturno reduce las tasas de predicción al 84%31.
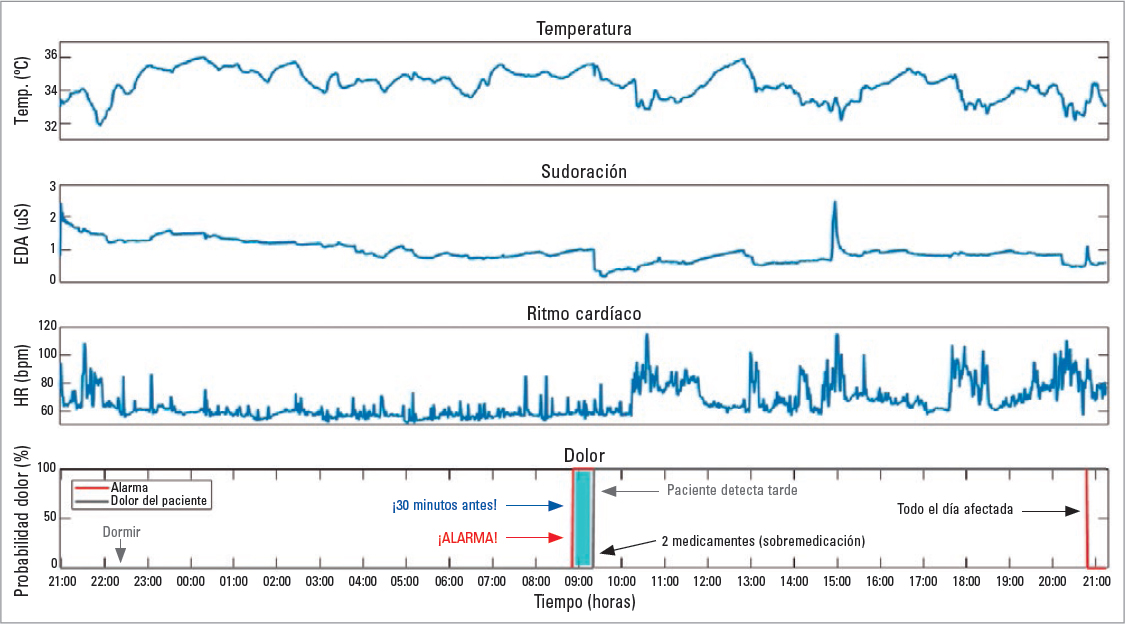
FIGURA 1. Representación del registro de diferentes variables biométricas con un dispositivo portátil. Registro inferior, zona central (dolor): se ejemplifica la posibilidad de detectar y avisar de la fase de dolor (línea roja) antes de la toma habitual de medicación (línea gris).
La pandemia por COVID-19 supuso un auge en la telemedicina y en el uso de aplicaciones móviles, también para el registro de las crisis de dolor en los usuarios con migraña. Este tipo de aplicaciones pueden incluir información meteorológica, tradicionalmente referida como un factor desencadenante importante en las crisis de migraña17. Así, se habría encontrado que la presión barométrica baja, los cambios de presión barométrica, la humedad más alta y la lluvia se asociaron con un mayor número de casos de dolor de cabeza en datos recogidos de 4.375 usuarios.
Algunas pruebas complementarias también podrían contribuir a la detección de las fases preictales. Este es el caso del electroencefalograma del estado de reposo, que podría detectar cambios dinámicos de la conectividad efectiva en las redes frontocentral y centroposterior18, con una mejora o «normalización» de la complejidad del electroencefalograma frontal durante la fase preictal en comparación con la fase interictal32.
INTELIGENCIA ARTIFICIAL EN LA PREDICCIÓN DE RESPUESTA A FÁRMACOS
En los últimos años, dadas la mejora en el diagnóstico y la aparición de nuevos fármacos, ha aumentado la necesidad de tener marcadores fiables de respuesta a los tratamientos que faciliten las políticas de financiación por los sistemas de salud. La IA se postula como una herramienta útil para obtener información y establecer planes de tratamiento personalizados con base en análisis de subgrupos y de efectividad comparativa.
Migraña
Los resultados de efectividad en cefaleas, al igual que ocurre en otras enfermedades que cursan con dolor crónico o en los trastornos del estado de ánimo, son a menudo catalogados como «suaves» en la medida que son, de alguna manera, predominantemente subjetivos. A pesar de ello, en migraña se ha podido demostrar que la IA aplicada a datos no estructurados puede identificar y simplificar características predictivas de respuesta terapéutica en la práctica clínica real19.
Recientemente, se ha obtenido un modelo predictivo de respuesta a anticuerpos anti-CGRP a los 6, 9 y 12 meses con datos de días de dolor de cabeza al mes, días de migraña al mes y puntuación en la escala HIT-6, con una precisión medida por F1 score de 0,7-0,9720.
Cefalea en racimos
En otras cefaleas, la aplicabilidad de modelos de IA en la predicción de respuesta terapéutica ha sido menos estudiada, si bien han surgido unos primeros modelos que combinan datos clínicos y de neuroimagen para predecir la respuesta a verapamilo en pacientes con cefalea en racimos, aunque con datos de precisión algo más modestos que en el caso de la migraña21.
CONCLUSIONES
La gran prevalencia de las cefaleas las convierte en un grupo de enfermedades muy atractivo para la IA y sus aplicaciones. En la última década, diferentes grupos de trabajo han tratado de mostrar la utilidad de estas herramientas, si bien la interpretación de estos resultados, a menudo opacos en la metodología y aplicados a pequeñas muestras de pacientes, debe interpretarse con cautela. Un diagnóstico precoz y más preciso de las distintas entidades permitirá reducir el tiempo hasta el diagnóstico, instaurar tratamientos efectivos de forma precoz y mejorar los algoritmos de derivación a los distintos niveles de atención especializada. Y, todo ello, en aras de un futuro de medicina personalizada con una «firma cerebral» específica de cada paciente con cefalea.
FINANCIACIÓN
La presente investigación no ha recibido ayudas específicas provenientes de agencias del sector público, sector comercial o entidades sin ánimo de lucro.
CONFLICTO DE INTERESES
Sonia Quintas ha recibido honorarios como ponente de Novartis, Lilly y Exeltis.
Alicia González Martínez ha recibido honorarios como ponente de TEVA.
Ana Beatriz Gago Veiga ha recibido honorarios como ponente o consultora de Novartis, Ei-Lilly, TEVA, Lundeck, Pfizer, Exeltis, Allergan-Abbvie y Almirall.
RESPONSABILIDADES ÉTICAS
Protección de personas y animales
Las autoras declaran que para este trabajo no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datos
Las autoras declaran que en este trabajo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informado
Las autoras declaran que en este trabajo no aparecen datos de pacientes.
Uso de inteligencia artificial para generar textos
Las autoras declaran que no han utilizado ningún tipo de inteligencia artificial generativa en la redacción de este manuscrito ni en la creación de figuras, gráficos, tablas o sus correspondientes pies o leyendas.
AGRADECIMIENTOS
Al Instituto de Salud Carlos III (ISCIII) y la European Union (ESF+) por la beca Río Hortega (CM21/00178) a A.G.M. y al ISCIII por el proyecto PMP 222/00158.